这次是乳腺癌领域!全球首创的“温江造”创新药迎来新进展

马年首个工作日,记者从温江企业四川百利天恒药业股份有限公司(以下简称“百利天恒”)获悉,由该企业自主研发的全球首创、新概念且唯一进入III期临床阶段的EGFR×HER3双抗ADC(iza-bren),在一项针对局部晚期或转移性三阴性乳腺癌(TNBC)的III期临床试验(研究编号:BL-B01D1-307)中,其预设的期中分析成功达到了PFS(无进展生存期)与OS(总生存期)双主要研究终点。


这是iza-bren作为全球首创双抗ADC药物,在乳腺癌领域取得的首个III期研究阳性结果;同时,它也是iza-bren第3项达到主要研究终点的III期临床研究。适应症为既往经紫杉烷类治疗失败的不可手术切除的局部晚期或转移性三阴性乳腺癌。
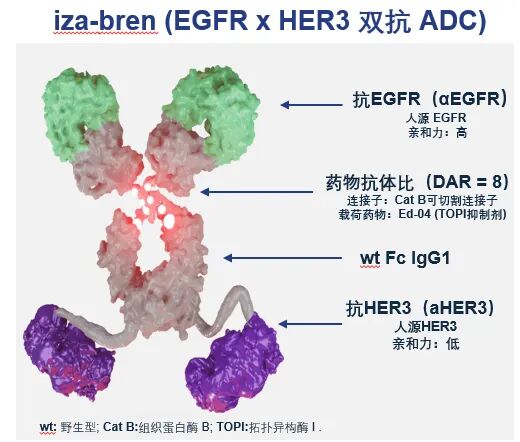
此项关键注册III期临床研究的成功,标志着iza-bren作为全球首创EGFR×HER3双抗ADC,在晚期三阴性乳腺癌领域取得重大突破,进一步拓宽了iza-bren的肿瘤适应症版图。
记者了解到,过去半年多来,iza-bren已有3项确证性注册III期临床研究达到主要终点,分别是:
2025年7月,iza-bren在鼻咽癌III期临床试验的期中分析达到主要研究终点;
2025年9月,被国家药品监督管理局药品审评中心(CDE)纳入优先审评,11月获正式受理;
2025年11月,iza-bren在食管鳞癌III期临床试验的期中分析取得PFS/OS双阳结果;
2026年1月获CDE正式受理并被纳入优先审评名单;以及此次在乳腺癌领域达到PFS和OS的双主要终点。

截至2026年1月,iza-bren正在中国和美国开展40余项针对多种肿瘤类型的临床研究,其中包括10项中国注册III期临床研究和3项全球关键注册临床研究。
凭借其突破性治疗潜力,iza-bren已有多个适应症获得中美监管部门的突破性治疗品种认定。在中国,非小细胞肺癌、小细胞肺癌、鼻咽癌、尿路上皮癌、食管癌、卵巢癌等7项适应症被国家药品监督管理局药品审评中心(CDE)纳入突破性治疗品种名单;在美国,非小细胞肺癌适应症被美国食品药品监督管理局(FDA)纳入突破性治疗品种名单。

百利天恒是一家在肿瘤大分子治疗领域(ADC/GNC/ARC)具备全球领先的创新研发能力、全球临床开发和规模化生产供应能力,并逐步发展成为具有全球商业化能力的综合型生物医药企业。2023年12月,其自主研发的iza-bren项目与百时美施贵宝(BMS)达成独家许可与合作协议,在全球范围内进行共同开发和商业化。

温江作为成都生物医药产业的主要承载地之一,已聚集上下游协作企业650余家,形成了“药械研发—生产制造—医疗应用”的完整产业生态。百利天恒正是温江持续深耕生物医药产业,加快培育“温江造”爆款创新药的生动缩影。目前,百利天恒共有17款创新药处于临床试验阶段,其中6款创新药处于全球临床试验,并在全球范围内开展100余项创新药临床试验。

记者:王戎 陈思洋
编辑:彭棣 钟诚
审核:高舒婷


评论